化妆品中莫匹罗星等5种组分的测定
发布时间:
按照化妆品补充检测方法BJH 202201《化妆品中莫匹罗星等5种组分的测定》,对莫匹罗星、夫西地酸、噻吗洛尔、特比萘芬、红霉素5种组分进行了测定。
按照标准方法对标准品、化妆水样品、乳液样品和面霜样品进行分析,并对实验中遇到的问题进行了简单的讨论,具体如下。

标准品分析结果
按照BJH 202201《化妆品中莫匹罗星等5种组分的测定》中方法,使用大阪曹達 CAPCELL PAK C18 MGII 色谱柱对莫匹罗星等5种组分标准品进行测定,得到结果如图1所示,5种组分分离及峰型良好。
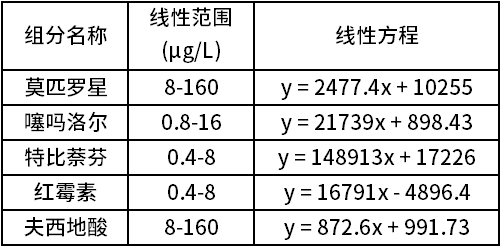
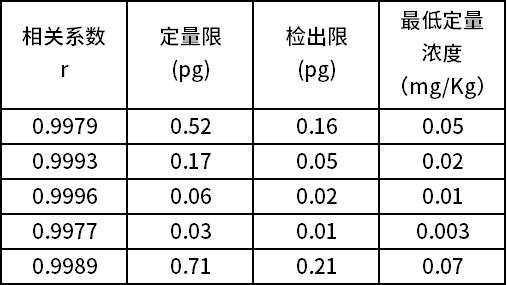
同时我们按照方法中要求,对5种组分系列浓度样品进行分析,得到线性范围、标曲、相关系数、检出限、定量限结果如表1所示。
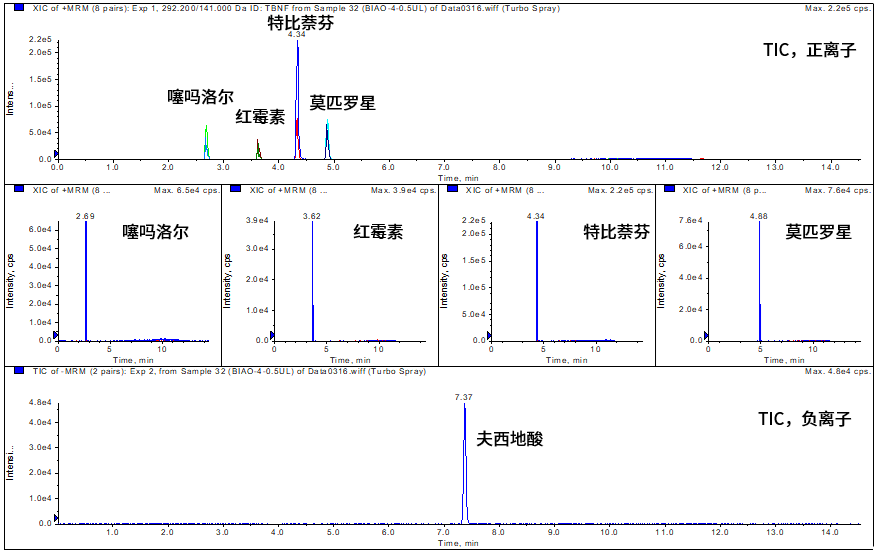
图1 莫匹罗星等5种组分标准谱图
表1 线性范围、标曲、相关系数
【色谱条件】
色谱柱:CAPCELL PAK C18 MGII S2; 2.0×100
流动相:A: 0.1%甲酸溶液 B: 乙腈
流动相:B% 10%(0 min)-85%(6 min)-95%(10 min)-10%(10.1 min)-10%(13.5 min)
流动速:0.3 mL / min
温动度:35 °C
检动测:SCIEX QTRAP 5500; MRM
浓动度:按照方法配置。
混合标准储备溶液:特比萘芬、红霉素浓度为4 mg/L,莫匹罗星、夫西地酸浓度为80 mg/L,噻吗洛尔浓度为8 mg/L的混合标准储备溶液(乙腈稀释)
系列浓度标准品溶液:准确量取混合标准储备溶液适量,置于10 mL棕色容量瓶中,用乙腈进行稀释,配制成混合标准系列溶液
进样量:0.5 µL
样品分析结果
按照方法,对化妆水、乳液、面霜3种不同基质样品进行了测定,结果分别如图2,3,4所示,化妆水中不含有莫匹罗星等5种组分,乳液、面霜样品虽然出现部分峰,但保留时间与标准品均不一致,该样品同样不含有莫匹罗星等组分。
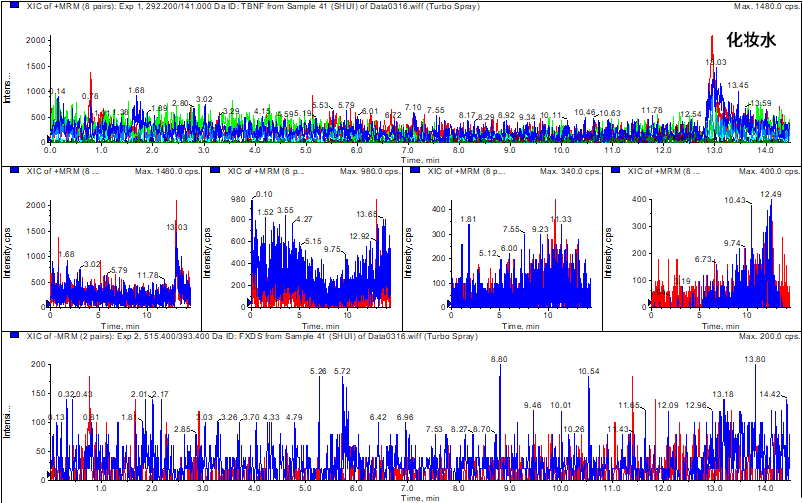
图2 化妆水样品分析结果
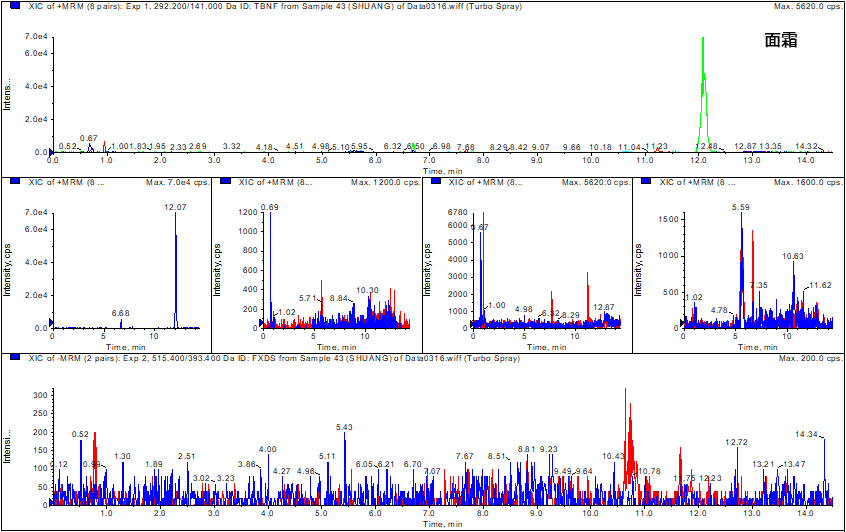
图3 面霜样品分析结果
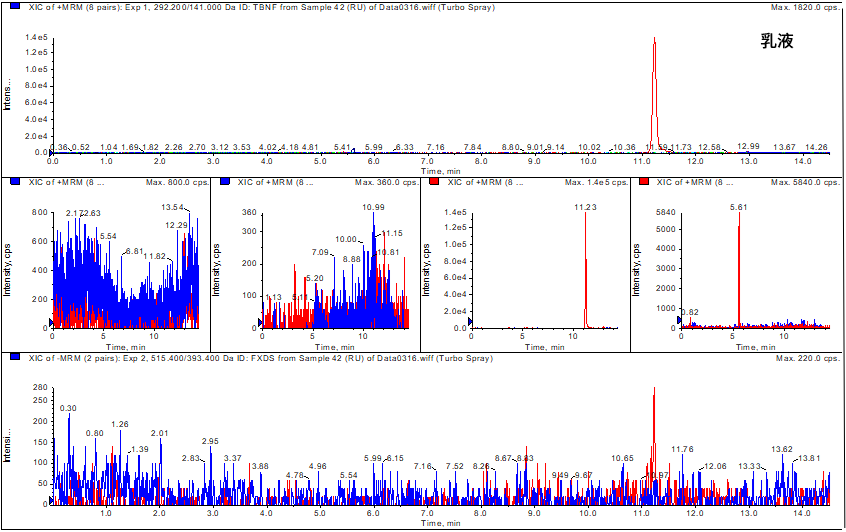
图4 乳液样品分析结果
【色谱条件】
色谱柱:CAPCELL PAK C18 MGII S2; 2.0×100
流动相:A: 0.1%甲酸溶液 B: 乙腈
流动相:B% 10%(0 min)-85%(6 min)-95%(10 min)-10%(10.1 min)-10%(13.5 min)
流动速:0.3 mL / min
温动度:35°C
检动测:SCIEX QTRAP 5500; MRM
浓动度:按照方法配置。
样品溶液:称取样品0.2 g,置于10 mL具塞比色管中,加入少量80%乙腈溶液,在涡旋混合仪上振荡30s至试样与提取溶剂混合均匀,然后加入80%乙腈溶液至近刻度,超声提取20 min,静置至室温,用80%乙腈溶液定容至刻度,摇匀,以10000 r/min离心10 min,取上清液经0.22 µm滤膜过滤后,滤液作为供试品溶液备用
进样量:0.5 µL
液相分析注意事项
1.原方法中进样量为1 µL,但由于样品及标准品均使用乙腈进行稀释或提取,在1 µL进样量下,会导致出峰较早的噻吗洛尔出现色谱峰前延问题,无法实现定量,如图5所示。
该问题的解决可通过两种方式:
1)降低进样量(本实验以0.5 µL进样时峰型正常)
2)使用初始比例流动相,再对标准品或样品进行稀释。
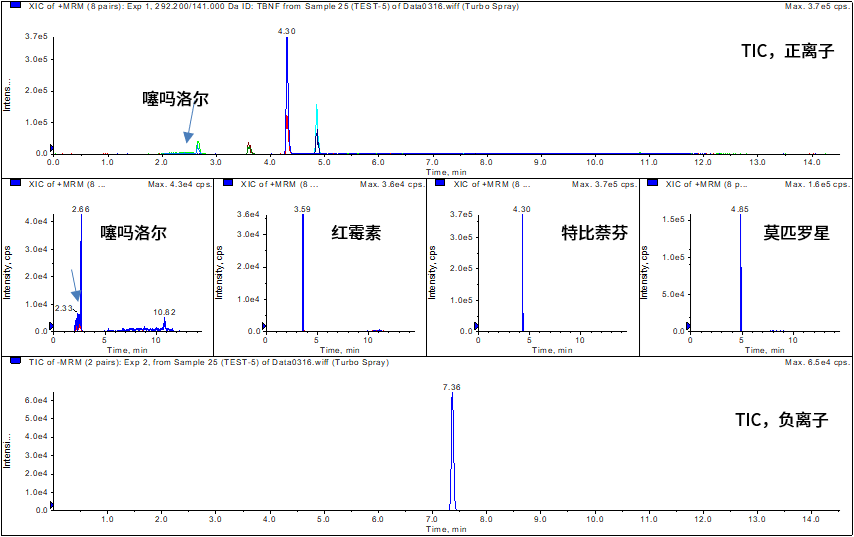
图5 溶剂效应导致峰型异常
2.在进样空白时发现,特比萘芬容易出现干扰峰,如图6所示,该干扰峰来源经排查为流动相,建议使用纯度级别较高的试剂或使用质谱兼容的鬼峰捕集小柱来消除流动相中干扰峰的存在。
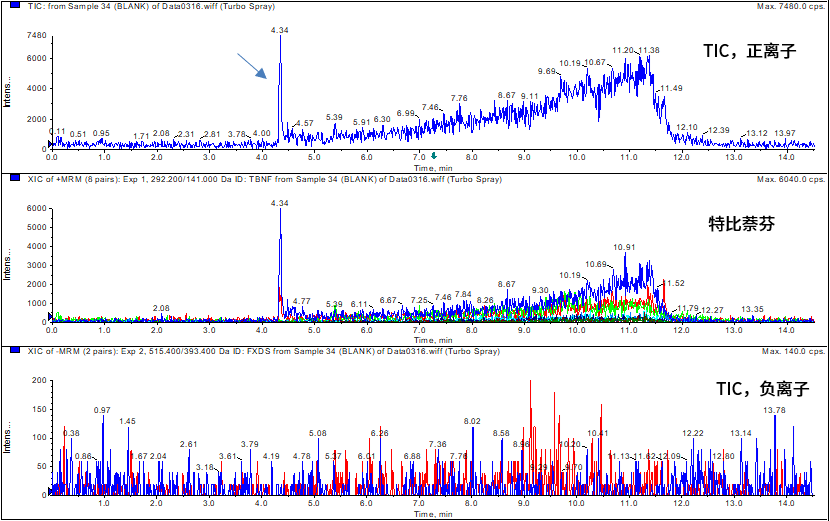
图6 干扰峰谱图
质谱条件
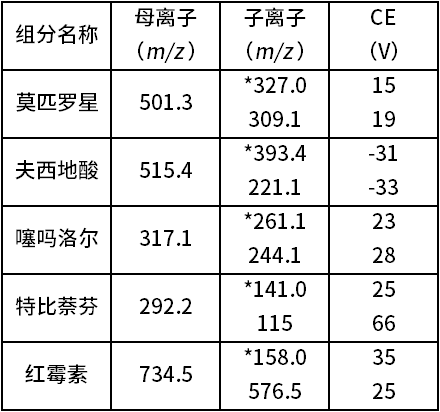
质谱检测条件使用方法中的参考条件,如表2所示,若定量限不能满足时,建议根据仪器情况进行质谱方法优化。
表2 莫匹罗星等5种组分监测离子对及相关参数设定
结论
综上所述,使用大阪曹達 CAPCELL PAK C18 MGII S2; 2.0mm i.d.×100mm色谱柱,按照化妆品补充检测BJH 202201《化妆品中莫匹罗星等5种组分的测定》方法,能够获得良好检测结果,满足标准要求。
化妆品补充检测(BJH 202201)
《化妆品中莫匹罗星等5种组分的测定》
推荐用柱 F94043
CAPCELL PAK C18 MGII S2; 2.0×100