8.1化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法 数据分享、分析注意事项和CP柱推荐
发布时间:
国家药品监督管理局发布了“国家药监局关于将油包水类化妆品的pH值测定方法等21项制修订项目纳入化妆品安全技术规范(2015年版)的通告(2023年第41号)”。
新增14项检验方法,纳入《化妆品安全技术规范(2015年版)》,自通告发布之日起实施。
今天给大家带来的是“化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法”的数据分享、分析注意事项和CP色谱柱推荐。
第一部分 化妆品中抗坏血酸磷酸酯镁等10种原料的检测
实验参照“化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法”,第一部分化妆品中抗坏血酸磷酸酯镁等10种原料的检测中方法,对抗坏血酸磷酸酯镁、抗坏血酸葡糖苷、苯乙基间苯二酚、4-丁基间苯二酚、4-甲氧基水杨酸钾、阿魏酸、烟酰胺、曲酸、3-邻-乙基抗坏血酸、鞣花酸10种组分进行了测定,并进行了面霜、乳液、粉底液样品的分析。
1 混合溶液的分析
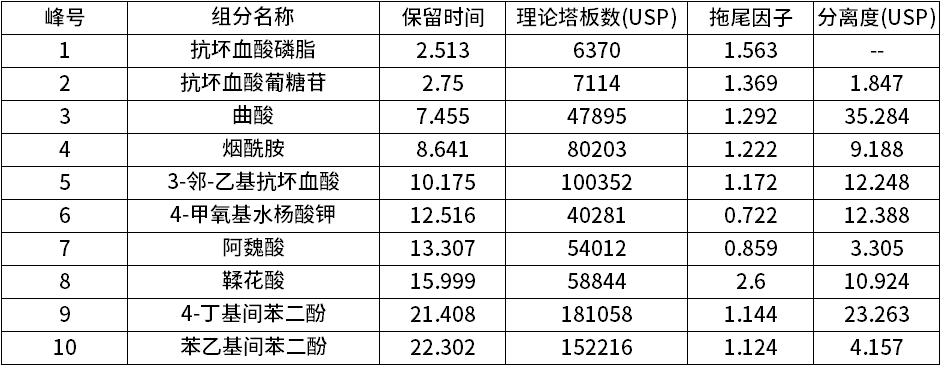
通过色谱柱筛选后,使用分离及峰形相对更好的CAPCELL PAK C18 MGII色谱柱进行了梯度优化,增加18-22min高比例有机相洗脱时间,对抗坏血酸磷酸酯镁等10种原料混合溶液进行分析,结果如图1~3、表1所示,10种原料均可达到分离度大于1.5的基线分离结果,分离良好。
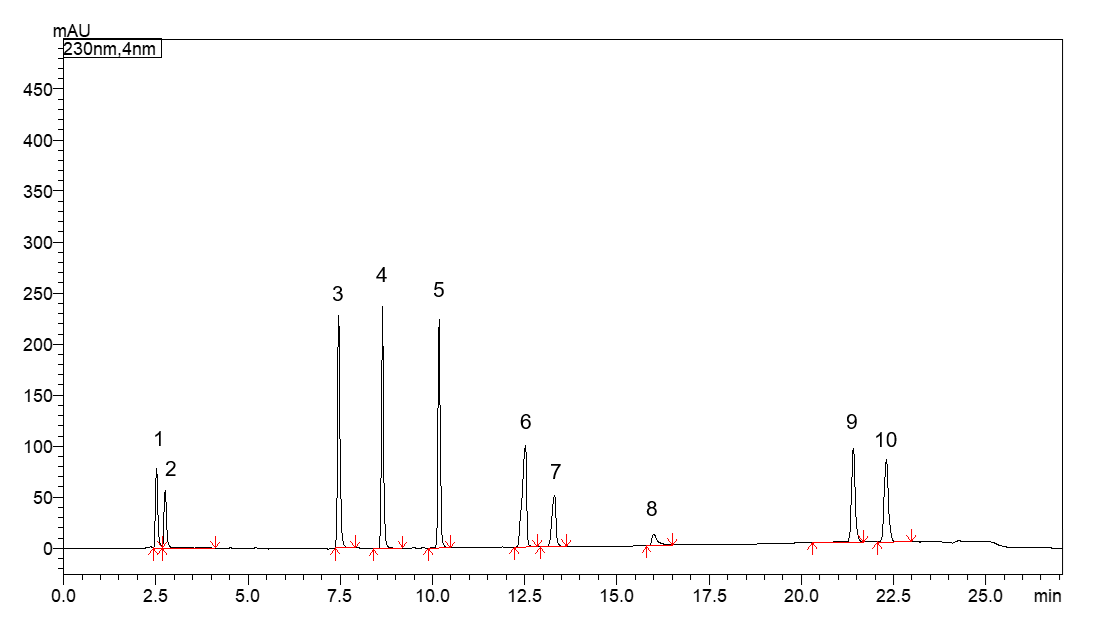
图1梯度调整后10种原料分析结果(230nm)
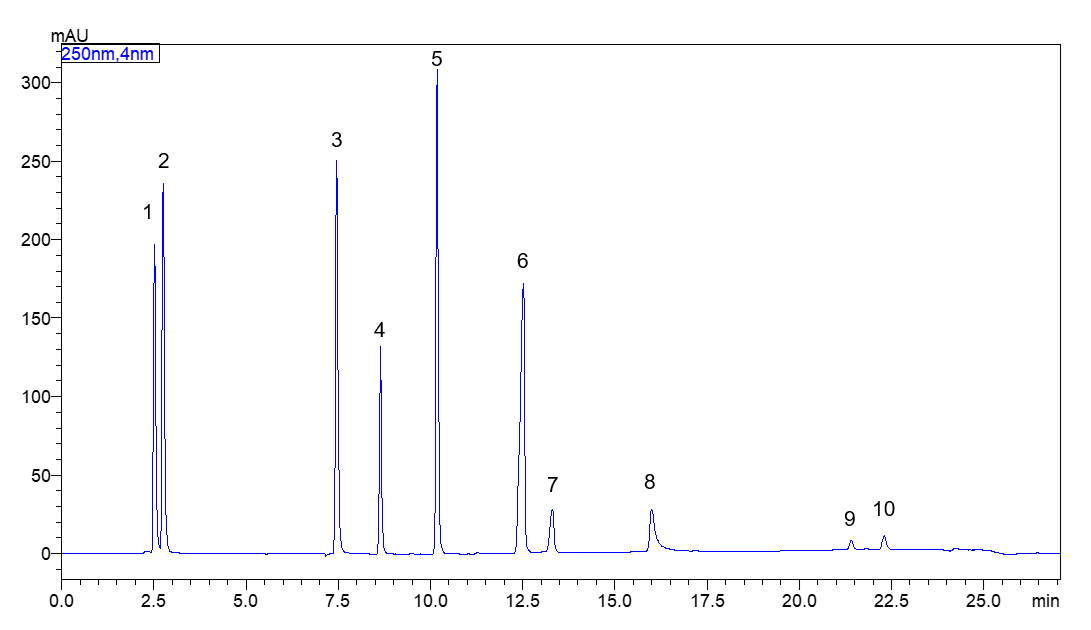
图2梯度调整后10种原料分析结果(250nm)

图3梯度调整后10种原料分析结果(280nm)
表1 10种原料分离结果(230nm条件积分结果)
【色谱条件】
色谱柱:CP C18 MGII S5; 4.6×250 mm
流动相:A:0.02 mol/L磷酸二氢钾溶液 B:甲醇
B% 5%(0 min)-5%(3 min)-40%(8 min)-60%(14 min)-70%(18 min)-70%(22 min)-5%(23 min)-5%(30 min)
流 速:1.0 mL/min
柱 温:25℃
检 测:PDA 230 nm; 250 nm; 280 nm
样 品:50 µg/mL(按照检验方法中5.1项配置)
进样量:10 μL
2 分析结果及方法学
2.1 线性实验的考察
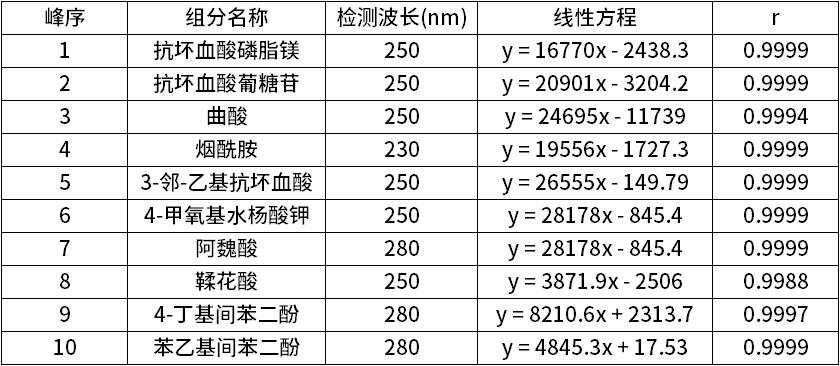
结果如表2所示,10种物质在不同范围内线性良好,相关系数均大于0.99,满足标准要求。
表2 线性范围考察
在上述条件下对乳液、面霜、粉底液化妆品样品进行分析,结果如图4~6所示,三个样品中均未检出10种原料峰。

图4 乳液样品分析结果
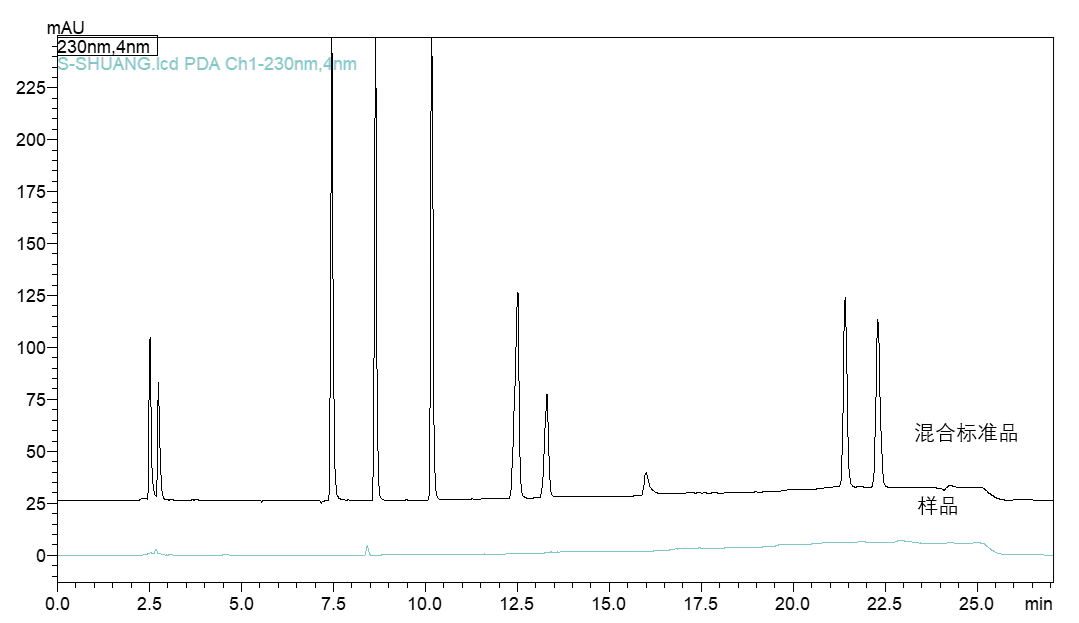
图5 面霜样品分析结果
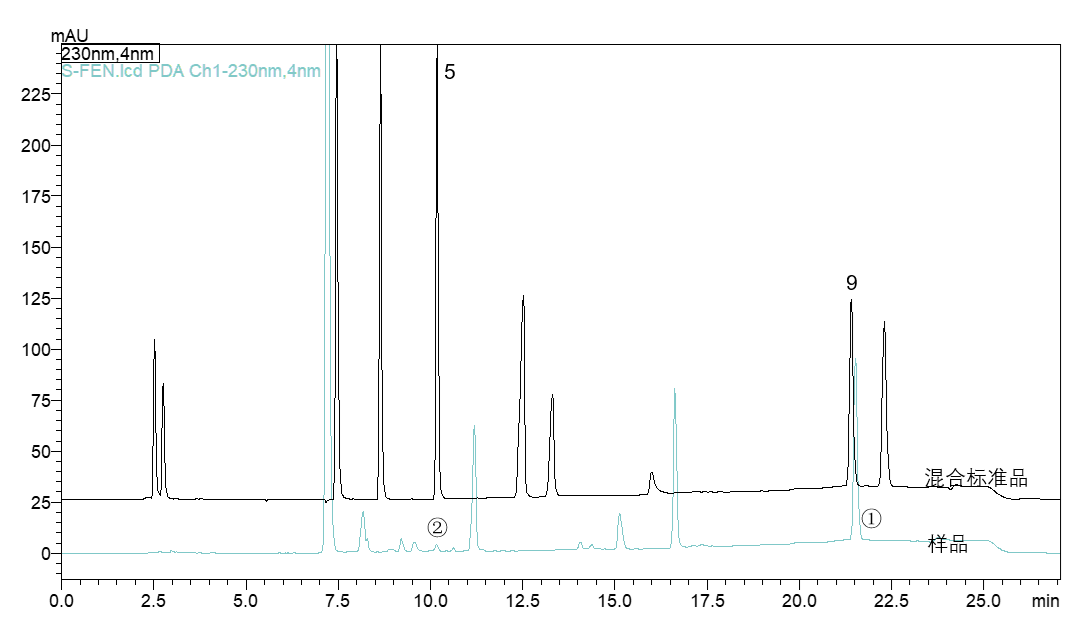
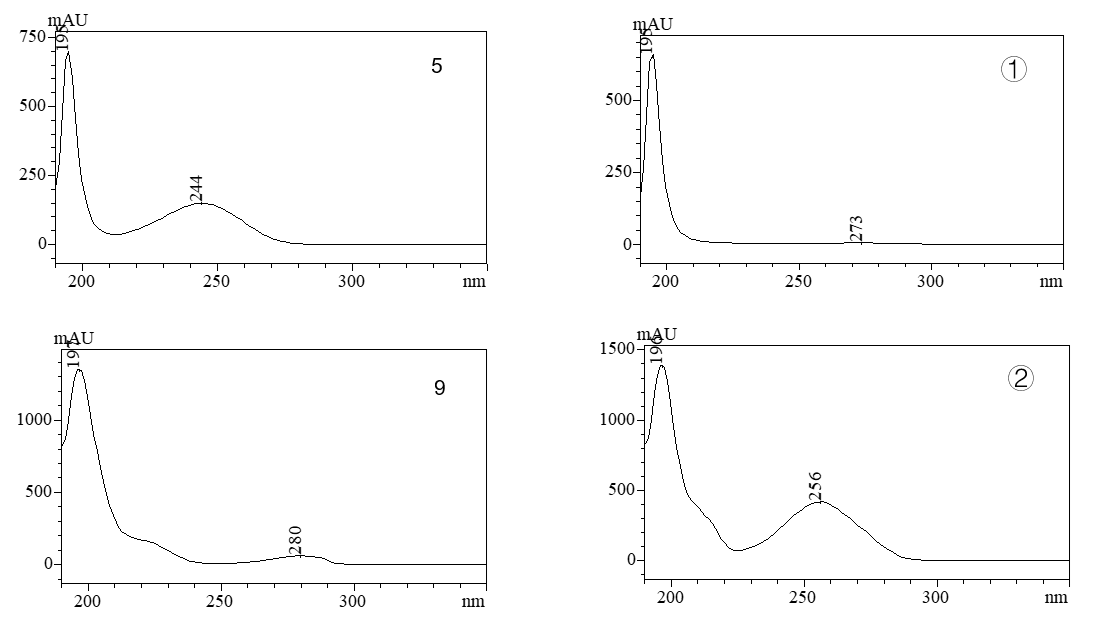
图6粉底液样品分析结果
3 分析注意事项
3.1色谱柱筛选
按照抗坏血酸磷酸酯镁等10种的检验方法,尝试使用不同极性的C18柱:CAPCELL PAK C18 MGII、CAPCELL PAK C18 AQ色谱柱,分别对抗坏血酸磷酸酯镁、抗坏血酸葡糖苷、苯乙基间苯二酚、4-丁基间苯二酚、4-甲氧基水杨酸钾、阿魏酸、烟酰胺、曲酸、3-邻-乙基抗坏血酸、鞣花酸10种组分进行分析。其中AQ色谱柱虽然保留时间长,但抗坏血酸磷酸酯镁峰型拖尾,导致与抗坏血酸葡糖苷分离较差,因此选择了CAPCELL PAK C18 MGII S5; 4.6×250 mm色谱柱进行后续分析。
3.2 梯度条件的调整
按照抗坏血酸磷酸酯镁等10种原料的原检验方法,苯乙基间苯二酚峰无法在梯度条件中良好洗脱,因此我们增加了70%甲醇的洗脱时间,已确保所有目标峰均被洗脱出来。由于不同仪器间存在延迟体积的不同,若遇到分离不好的情况,需要进行梯度条件的微调。
流动相:A:0.02 mol/L磷酸二氢钾溶液 B:甲醇
原梯度条件:B% 5%(0 min)-5%(3 min)-40%(8 min)-60%(14 min)-70%(18 min)-5%(25 min)-5%(30 min)
优化后梯度条件:B% 5%(0 min)-5%(3 min)-40%(8 min)-60%(14 min)-70%(18 min)-70%(22 min)-5%(23 min)-5%(30 min)
3.3 对于有基质干扰的样品,可考虑通过光谱图比对,或调整流动相条件进行分离等方式排查。
4 结论
综上所述,使用CAPCELL PAK C18 MGII S5; 4.6×250 mm色谱柱,在新化妆品检测方法“化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法”第一部分化妆品中抗坏血酸磷酸酯镁等10种原料的检测中方法基础上微调梯度后,能够获得良好检测结果,满足标准要求。
第二部分 化妆品中凝血酸(氨甲环酸)的检测
实验参照“化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法”,第二部分化妆品中凝血酸(氨甲环酸)的检测中方法,对氨甲环酸组分进行了测定,并进行了化妆水、乳液样品的分析。
1 标准品分析
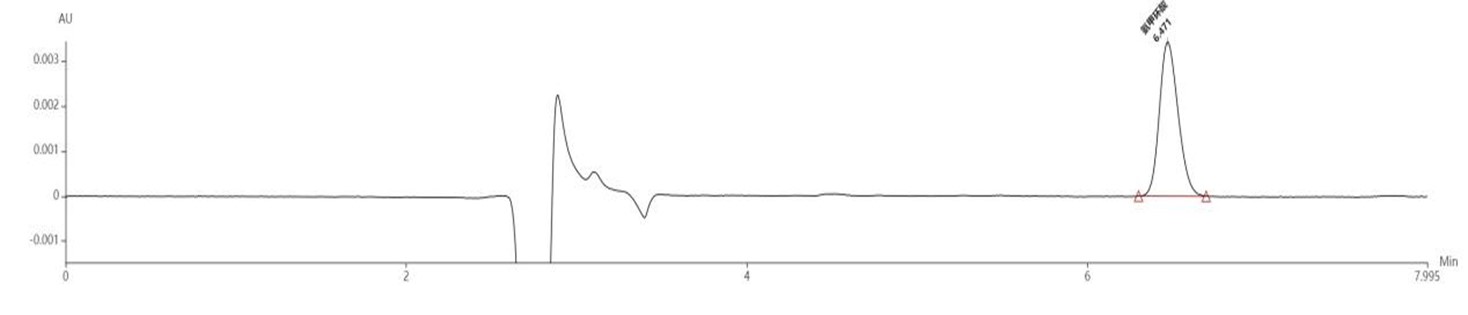
该方法中有机相比例仅为5%,因此选择可在100%水相中稳定使用的CAPCELL PAK C18 AQ色谱柱进行分析,得到结果如图1所示,氨甲环酸标准品保留时间6.47 min,理论塔板数16557,拖尾因子1.17。
同时我们也用水逐级稀释标准品至五个系列浓度:5 µg/mL,10 µg/mL,20 µg/mL,50 µg/mL,100 µg/mL,测定标准曲线,线性良好,r=0.9992,线性方程为y = 249.89x。
以线性最低浓度计算检出限为17.2 ng。
【色谱条件】
色谱柱:CP C18 AQ S5; 4.6×250 mm
流动相:A:0.05 mol/L KH2PO4-0.2% H3PO4溶液 B:甲醇
A:B = 95:5
流 速:1 mL/min
温 度:30 °C
检 测:UV 210 nm
浓 度:100 µg/mL(水溶)
进样量:20 µL
2 样品分析
按照检验方法,对化妆水、乳液2种不同基质样品进行了测定,结果如图2所示,在化妆水样品中存在一定基质干扰峰,我们在化妆水样品中加入标准品,得到谱图如图3所示,基质干扰峰与氨基环酸峰分离度不足1.5,会影响定量结果。
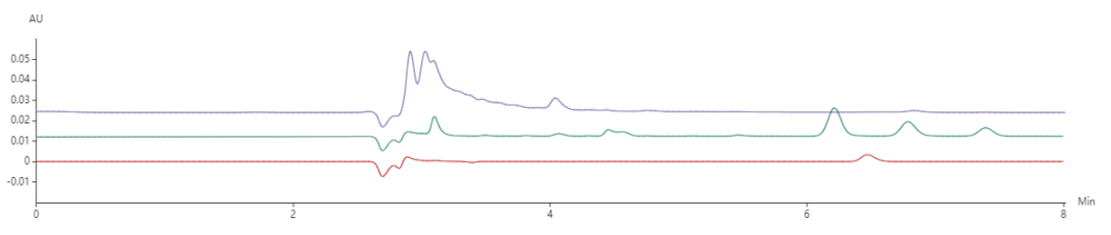
图2 样品分析结果(从下至上:标准品、化妆水、乳液)
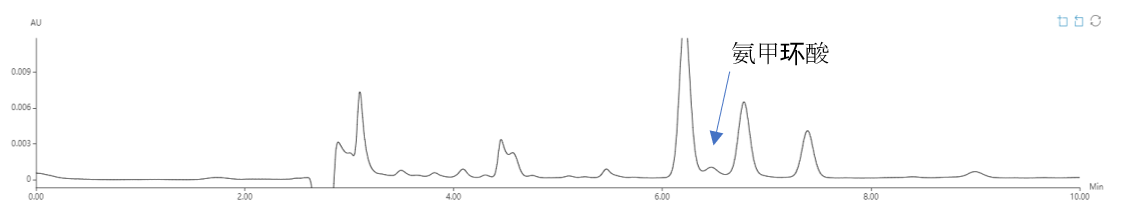
图3 化妆水样品加标分析结果
【色谱条件】
色谱柱:CP C18 AQ S5; 4.6×250 mm
流动相:A:0.05 mol/L KH2PO4-0.2% H3PO4溶液 B:甲醇
A:B = 95:5
流 速:1 mL/min
温 度:30 °C
检 测:UV 210 nm
浓 度:样品处理:准确称取化妆品试样0.5 g于15 mL具塞比色管中,加入5 %甲醇溶液至约9 mL,涡旋振荡使试样与提取溶剂充分混匀,超声提取10 min,冷却至室温。转移至10 mL容量瓶中,加5 %甲醇溶液定容至刻度,混匀后转移至离心管中,以12000 r/min的转速离心10 min。上清液经孔径0.22 µm的滤膜过滤后,滤液作为样品待测溶液。
进样量:20 µL
由于部分样品存在基质干扰,因此在原分析条件基础上,进行了方法调整。
一方面降低了流动相中有机相比例,延长氨甲环酸保留时间至10 min以上;
另外也加入了梯度洗脱,以便将样品基质中的疏水性物质进行冲洗,更加有利于分析方法整体的稳定性及提高色谱柱寿命。
同时对该加标样品进行了回收率测试,回收率为102.86%。
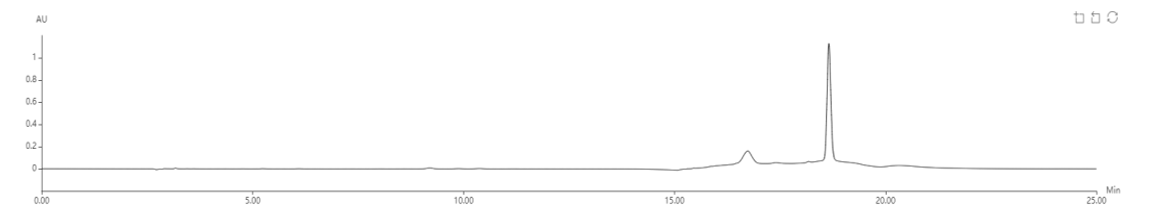
图4 方法调整后分析结果
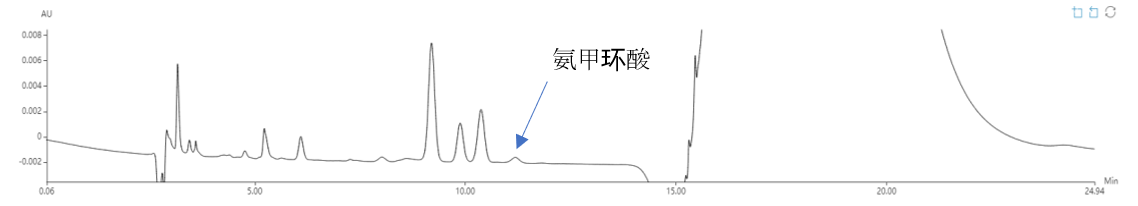
图5 方法调整后分析结果局部放大图
【色谱条件】
色谱柱:CP C18 AQ S5;4.6×250 mm
流动相:A:0.05 mol/L KH2PO4-0.2% H3PO4溶液 B:甲醇
B% 0%(0 min)-0%(10 min)-60%(12 min)-60%(15 min)-0%(16 min)-0%(25 min)
流 速:1 mL/min
温 度:30 °C
检 测:UV 210 nm
浓 度:样品处理:准确称取化妆品试样0.5 g于15 mL具塞比色管中,加入5 %甲醇溶液至约9 mL,涡旋振荡使试样与提取溶剂充分混匀,超声提取10 min,冷却至室温。转移至10 mL容量瓶中,加5 %甲醇溶液定容至刻度,混匀后转移至离心管中,以12000 r/min的转速离心10 min。上清液经孔径0.22 µm的滤膜过滤后,滤液作为样品待测溶液。
进样量:20 µL
3 分析注意事项
由于该方法水相比例较高,建议选择耐水性能良好的C18色谱柱进行分析;
对于有基质干扰的样品,可考虑通过光谱图比对,或调整流动相条件进行分离等方式进行排查。
4 结论
综上所述,使用CAPCELL PAK C18 AQ S5; 4.6×250mm色谱柱,在新化妆品检测方法“化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法”,第二部分化妆品中凝血酸(氨甲环酸)的检测方法,能够获得良好检测结果,满足标准要求。